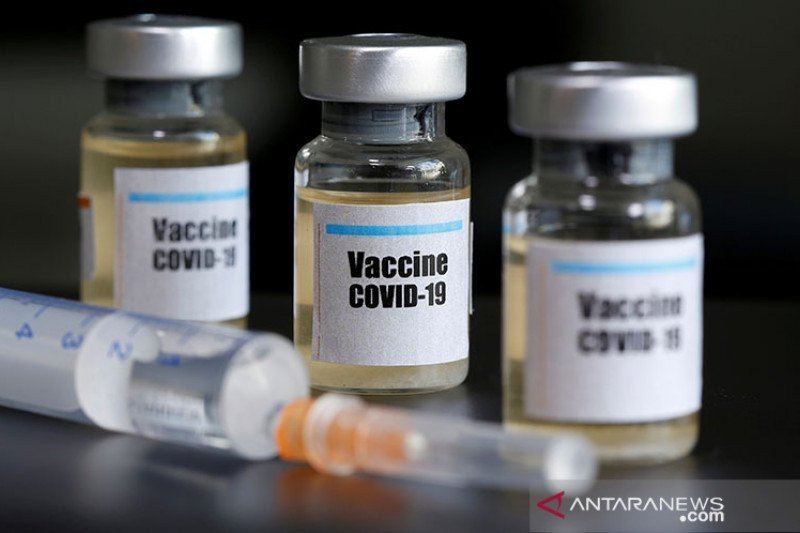
Vaksin yang datang beberapa waktu lalu ini, masih memerlukan beberapa tahapan lagi sebelum bisa dilakukan uji klinis pada Agustus 2020 mendatang. Tahap yang masih harus dilewati tersebut antara lain pengujian di dalam Laboratorium Bio Farma, dan beberapa perizinan lainnya.
Uji klinis vaksin COVID-19 itu, akan dilaksanakan di Pusat Uji Klinis yaitu di Fakultas Kedokteran UNPAD, yang akan mengambil contoh sebanyak 1.620 subjek dengan rentang usia antara 18 – 59 tahun, dengan kriteria – kriteria tertentu. Sedangkan sisa dari vaksin tersebut, akan digunakan untuk uji lab di beberapa lab antara lain di Bio Farma dan Pusat Pengujian Obat Dan Makanan Nasional (PPOMN).
Direktur Utama Bio Farma, Honesti Basyir mengatakan, uji klinis tahap 3 vaksin COVID-19, dijadwalkan akan berjalan selama enam bulan, sehingga ditargetkan akan selesai pada bulan Januari 2021.
Baca juga: Kementerian BUMN optimistis uji klinis vaksin COVID-19 akan berhasil
Apabila uji klinis vaksin COVID-19 tahap 3 lancar, maka Bio Farma akan memproduksinya pada kuartal pertama 2021 mendatang, dan Bio Farma sudah mempersiapkan fasilitas produksinya dengan kapasitas produksi maksimal di 250 juta dosis.
Tentu saja upaya uji klinis ini bisa dibilang sebagai tindakan atau aksi luar biasa (extraordinary) yang memang diharapkan oleh Presiden Joko Widodo untuk menghadapi masa krisis yang begitu genting seperti sekarang.
Skenario cepat dan matang Bio Farma
Proses mendatangkan vaksin Sinovac China bukanlah sebuah proses instan atau mendadak ada, melainkan sebuah bagian dari skenario yang telah direncanakan amat matang oleh Bio Farma ketika pandemi COVID-19 melanda Tanah Air dalam rangka menyelamatkan masyarakat Indonesia.
Direktur Pemasaran, Penelitian & Pengembangan Bio Farma Sri Harsi Teteki mengungkapkan bahwa terkait vaksin COVID-19, Bio Farma memang telah memiliki beberapa skenario yakni skenario jangka pendek atau cepat (quick win) dan skenario jangka panjang.
Baca juga: Bio Farma siap produksi vaksin COVID-19 hingga 100 juta dosis
Untuk skenario jangka panjang, Bio Farma bersama dengan lembaga Eijkman yang ditunjuk oleh pemerintah dalam hal ini untuk mencari vaksin tersebut. Bio Farma menunggu hasil riset dari lembaga Eijkman yang diharapkan pada awal 2021 ditemukan bibit vaksin COVID-19 yang dapat diberikan kepada Bio Farma untuk kemudian menjalani uji klinis mulai dari tahap 1 hingga 3.
Kendati demikian, Sri Harsi Teteki menilai kemungkinan dengan skenario jangka panjang ini di mana Indonesia membuat vaksin dari nol maka diperkirakan vaksin COVID-19 buatan Indonesia baru selesai menjalani seluruh uji klinis dan hadir pada akhir tahun 2021.
Karena skenario jangka panjang ini ternyata diperkirakan membutuhkan waktu yang lama terkait produksi vaksin, maka Bio Farma berupaya mati-matian mencari cara agar bagaimana pun juga vaksin COVID-19 harus segera hadir di Indonesia dalam rangka secepat mungkin menyelamatkan waktu masyarakat Indonesia.
Melalui skenario quick win, Bio Farma bekerjasama dengan lembaga dan perusahaan internasional untuk segera mendapatkan vaksin COVID-19. Bio Farma kemudian berupaya menjalin kerjasama dengan dua lembaga/perusahaan internasional yakni The Coalition for Epidemic Preparedness Innovations (CEPI) Norwegia dan perusahaan farmasi Sinovac asal China.
Dan seperti diketahui bersama, Bio Farma kemudian berhasil mendatangkan vaksin COVID-19 dari Sinovac China yang kemudian akan menjalani uji klinis.
Harapan dalam mengendalikan COVID-19
Mungkin banyak masyarakat Indonesia yang penasaran apa sebetulnya kandungan vaksin COVID-19 dari Sinovac China tersebut.
Menurut dokumen "DRAFT landscape of COVID-19 candidate vaccines" yang dilansir dari situs WHO, vaksin COVID-19 dari Sinovac China menggunakan Inactivated + alum.
Ahli kesehatan publik dari lembaga kajian Think Policy Society, Egi Abdul Wahid menilai bahwa kandungan Inactivated + alum dalam vaksin Sinovac merupakan virus yang sudah di Inaktivasi atau dibuat tidak aktif namun tidak menghilangkan sifat antigennya.
Menurut Egi, WHO sendiri telah mencatat bahwa terdapat 24 calon vaksin COVID-19 dan ada empat perusahaan yang sudah masuk tahap uji klinis tahap III, di mana tiga perusahahaan tercatat dari China, dan satu lagi dari Universitas Oxford di Inggris. Sinovac sendiri merupakan salah satu dari tiga perusahaan China pembuat vaksin COVID19 yang sudah memasuki uji klinis tahap 3.
Terkait arti dan maksud uji klinis tahap 3 vaksin COVID-19, untuk memastikan vaksin yang diberikan ke masyarakat itu memiliki tingkat efektivitas dan keamanan yang baik, Dunia menetapkan kriteria yang ketat dalam memproduksi
vaksin.
Egi menilai uji klinis tahap 3, merupakan tahapan terakhir yang harus dilakukan oleh pengembang vaksin. Bagi Indonesia dan bahkan Dunia ini tentu menjadi harapan dalam mengendalikan COVID-19.
Sedangkan Staf Khusus Menteri BUMN, Arya Sinulingga mengatakan bahwa pihaknya memang berharap nanti setelah melalui uji klinis yang ada dan dites nanti, maka vaksin tersebut bisa diproduksi juga di indonesia.
Seperti diketahui virus yang ada di Indonesia merupakan virus yang memang bisa saja berbeda dengan yang ada di China dan itu yang BUMN lakukan dengan menjalankan tes genis terlebih dahulu, apakah vaksin ini memang cocok dan bisa mematikan virus Corona yang ada di indonesia.
"Saya mendapatkan informasi bahwa vaksin Sinovac agak berbeda dengan vaksin yang lain karena dia agak melebar, dia agak bisa untuk beberapa jenis virus corona yang berkembang. Jadi dicoba di China juga, dan saat ini kita lagi proses juga mencoba vaksin itu," kata Arya Sinulingga.
100 juta dosis per tahun
Bio Farma sendiri mengaku siap memproduksi vaksin COVID-19 hingga 100 juta dosis per tahun. Rencananya BUMN produsen vaksin tersebut akan memproduksi dan mendistribusikan vaksin tersebut bila uji klinis berhasil.
Bio Farma sendiri berencana akan melakukan ekspansi menuju 250 juta dosis per tahun tapi untuk tahap pertama sesuai target penyelesaian uji klinis Januari 2021, pada saat selesai uji klinis dan izin edarnya keluar, kami sudah menargetkan untuk bisa selesai sekitar 40 juta dosis per tahun.
Saat ini, vaksin dari Sinovac tersebut menurut Direktur Utama Bio Farma Honesti Basyir, berada di Biofarma dan masih disimpan sesuai dengan ketentuan-ketentuan penyimpanan vaksin internasional.
Ketika uji klinis sudah dimulai Bio Farma akan memberikan kepada tim uji klinis untuk segera diberikan vaksinasi ke sampel sejumlah 1.620 orang, dan uji klinis tersebut rencananya akan dilakukan di Bandung dan sekitarnya yang akan dilakukan oleh tim peneliti dari Universitas Padjajaran.
Terkait rencana uji klinis tahap 3 dan produksi 100 juta dosis vaksin COVID-19 ini, pengamat BUMN Toto Pranoto meminta publik untuk tidak meragukan kemampuan Bio Farma sebagai BUMN penghasil vaksin.
Menurut Toto, Bio Farma merupakan perusahaan yang berusia lebih dari 100 tahun . Bio Farma juga dinilai sebagai "prominent company" dalam menghasilkan vaksin , telah diakui WHO dan semua lembaga internasional serta telah melakukan ekspor ke lebih dari 100 negara. Dengan latar belakang seperti ini tidak ada keraguan bahwa Bio Farma akan mampu melakukan uji klinis tahap 3 dengan baik.
Kendati demikian pengamat BUMN tersebut menyarankan agar perlunya kerjasama dan koordinasiu kuat yang dilakukan Bio Farma bersama perguruan tinggi , pemerintah daerah, BPOM dan para pemangku kepentingan lainnya supaya uji klinis tahap 3 bisa dilakukan dengan cepat namun sesuai SOP yang ada.
Pewarta: Aji Cakti
Editor: Budi Suyanto
Copyright © ANTARA 2020