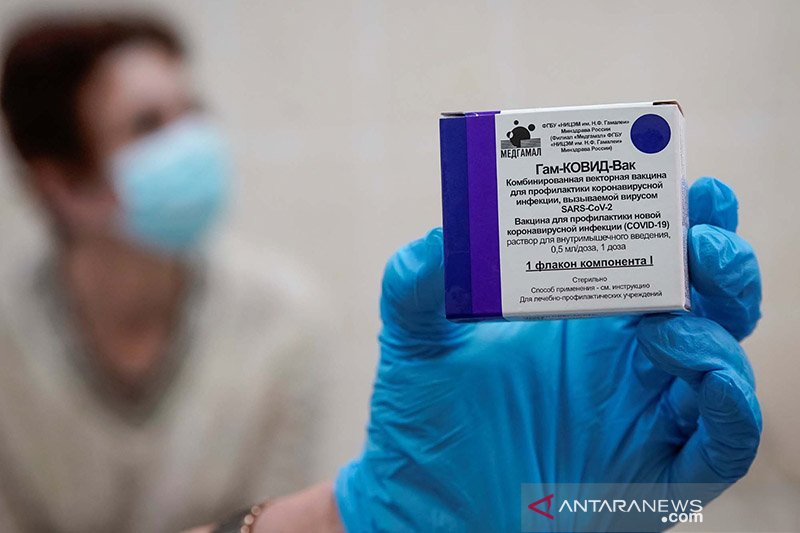
Dalam sebuah pernyataan di laman daring Kementerian Kesehatan, Anvisa menyebut bahwa permintaan perusahaan itu gagal memberikan jaminan yang cukup meyakinkan atas uji klinis fase ke-III dan sejumlah isu terkait produsen vaksin.
Para pejabat Anvisa telah mengatakan bahwa vaksin Sputnik V akan harus melalui fase ke-III uji klinis di Brazil sebelum penggunaannya dapat diotorisasi.
Dalam pernyataannya, Anvisa juga mengatakan bahwa siapapun yang mengajukan izin penggunaan darurat harus menunjukkan uji klinis vaksin yang tengah berlangsung akan membawa keamanan dan kemanjuran jangka panjang.
Uniao Quimica meminta persetujuan untuk penggunaan 10 juta dosis Sputnik V di Brasil pada kuartal pertama tahun ini.
Anvisa diperkirakan akan memutuskan untuk mengotorisasi penggunaan darurat vaksin yang dikembangkan oleh Sinovac China dan AstraZeneca Inggris pada hari Minggu.
Sumber: Reuters
Baca juga: Pakar cukup puas hasil uji Sinovac di Brazil
Baca juga: Anvisa Brazil: Permohonan vaksin COVID Sinovac China minim informasi
Baca juga: Rusia akan ajukan izin pemakaian vaksin Sputnik V ke Uni Eropa
Pewarta: Aria Cindyara
Editor: Atman Ahdiat
Copyright © ANTARA 2021