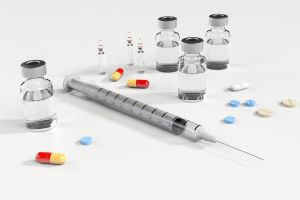
Wabah virus corona yang belum sepenuhnya bisa dikendalikan oleh pemerintah di berbagai negara memacu proses pembuatan vaksin.Tidak boleh dipercepat karena nanti akhirnya tidak baik, malah vaksin ini tidak terpantau efek sampingnya dan manfaatnya
Pemerintah sejumlah negara bersama ilmuwan kesehatan dan perusahaan farmasinya seperti sedang berlomba menjadi yang tercepat. Tujuannya menghasilkan vaksin untuk mengatasi wabah yang bermula dari Wuhan (China) ini.
Kolaborasi atau kerja sama juga dilakukan oleh beberapa negara. Tujuannya menghasilkan vaksin yang sangat didambakan di tengah wabah ini.
Bagaimana dengan Indonesia? Seberapa mampu untuk berperan?
Baca juga: Gerak cepat Bio Farma hadirkan vaksin demi kendalikan pandemi COVID-19
Kalangan ilmuwan di perguruan tinggi di Indonesia diyakini telah mengambil perannya untuk terlibat dalam mengatasi wabah ini. Terkait vaksin, misalnya, beberapa dari ilmuwan itu telah melakukan penelitian.
Demikian pula dengan pemerintah yang terus mendorong terwujudnya vaksin virus corona tipe baru (COVID-19). Itu dilakukan dengan mendorong ilmuwan kesehatan maupun kerja sama dengan pihak luar negeri.
Salah satunya adalah kerja sama pengembangan vaksin antara BUMN farmasi, yakni Bio Farma dengan Sinovac Biotech dari China. Kerja sama itupun sudah sampai tahap pengujian sampel kandidat vaksin.
Dalam kaitan ini, sebanyak 2.400 sampel kandidat vaksin COVID-19 dari Sinovac sudah tiba di Indonesia pada Ahad (19/7). Sinovac menggandeng Bio Farma dan Universitas Padjadjaran (Unpad) Bandung untuk menguji klinis tahap III sampel kandidat vaksin itu.
Baca juga: Kementerian BUMN optimistis uji klinis vaksin COVID-19 akan berhasil
Puskesmas
Bukan hanya dengan Bio Farma uji klinis tahap III atas kandidat vaksin itu dilakukan. Namun juga dengan beberapa negara.
Uji klinis tahap III kandidat vaksin COVID-19 dari Sinovac itu dikerjakan bersama-sama dengan India, Bangladesh, negara-negara Afrika dan Amerika Latin termasuk Brazil. Di Timur Tengah dengan Persatuan Emirat Arab (Uni Emirat Arab/UEA).
Rencananya, uji klinis tahan III dimulai Agustus 2020 hingga Januari 2021. Bila berhasil, Bio Farma mulai memproduksinya pada kuartal pertama 2021.
Manajer Lapangan Uji Klinis Vaksin COVID-19 dari Fakultas Kedokteran Universitas Padjadjaran (Unpad) Dr Eddy Fadlyana SpA(K) MKes mengatakan uji klinis tahap ketiga III akan dilakukan di enam tempat di Kota Bandung. Yakni empat Puskesmas ditambah Balai Kesehatan Unpad dan Rumah Sakit Pendidikan (RSP) Unpad.
Keempat Puskesmas di Kota Bandung yang akan dijadikan lokasi uji coba ialah Puskesmas Garuda, Puskesmas Ciumbeuleuit, Puskesmas Dago, dan Puskesmas Puter.
Uji klinis ini melibatkan 1.620 relawan yang lolos seleksi. Mereka berusia 18-59 tahun dan harus sehat serta dijamin asuransi.

Di enam lokasi tempat penelitian dan uji klinis itu juga sudah dilakukan pelatihan. Pelatihan di tempat-tempat tersebut melibatkan tim dokter umum dengan 30 hingga 40 orang.
Selain dokter umum, juga direkrut dokter spesialis penyakit dalam dan dokter spesialis penyakit anak. Ada juga ahli lainnya sesuai dengan kebutuhan dari penelitian ini.
Baca juga: Bio Farma siap produksi vaksin COVID-19 hingga 100 juta dosis
Siap Produksi
Kalau berhasil, PT Bio Farma siap memproduksi vaksin COVID-19 hingga 100 juta dosis per tahun. Bio Farma mendapat tugas untuk memastikan kapasitas produksi vaksin ini bisa dikelola dengan baik.
Ke depan, Bio Farma mengklaim mampu memproduksi 250 juta dosis per tahun. Tapi untuk tahap pertama sesuai target penyelesaian uji klinis Januari 2021 dan pada saat selesai uji klinis serta izin edarnya keluar, sudah ditargetkan untuk bisa memproduksi sekitar 40 juta dosis per tahun.
Saat ini, kandidat vaksin dari Sinovac tersebut berada di Bio Farma. Barang itu masih disimpan sesuai dengan ketentuan-ketentuan penyimpanan vaksin internasional.
"Saatnya nanti uji klinis dimulai saya akan berikan ke tim uji klinis untuk segera diberikan vaksinasi ke sampel sejumlah 1.620 orang," ungkap Dirut Bio Farna Honesti Basyir.
Ketua Tim Peneliti Uji Klinis Vaksin COVID-19 dari Fakultas Kedokteran Universitas Padjadjaran (Unpad) Prof Dr Kusnandi Rusmil Sp AK MM mengemukakan uji klinis tahap III ditargetkan selesai pada Januari 2021.
Artinya butuh waktu enam bulan jika dihitung dari dimulainya uji klinis tahap III, yakni Agustus 2020. Uji klinis tidak bisa dipercepat, misalnya, tiga bulan karena harus dilakukan dengan hati-hati dan benar sesuai tata cara yang sudah diatur WHO.
"Tidak boleh dipercepat karena nanti akhirnya tidak baik, malah vaksin ini tidak terpantau efek sampingnya dan manfaatnya," kata Kusnandi.
Uji tahap klinis I dan II dilakukan di China dengan hasil yang baik. Sekarang uji klinis ketiga dilakukan di beberapa negara dengan harapan hasilnya baik sehingga vaksin ini bisa dipergunakan.
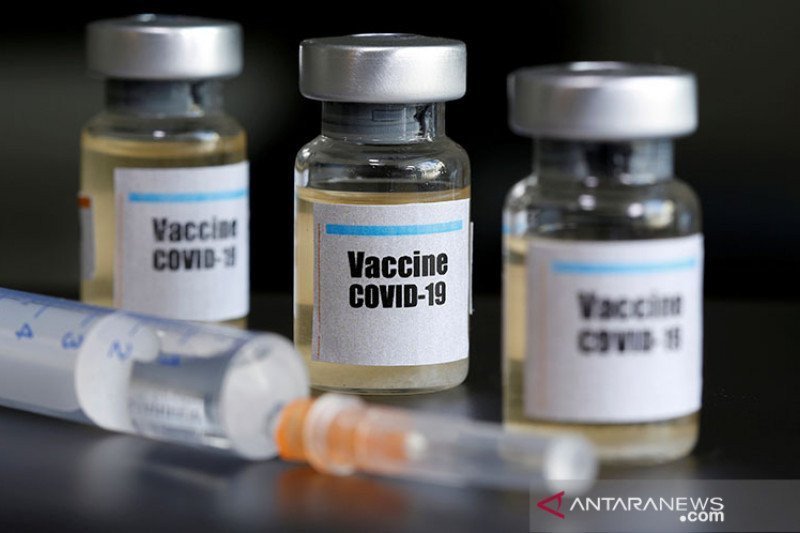
Harapan
Kini publik menunggu hadirnya vaksin virus corona. Harapan juga layak disampaikan agar vaksin yang dihasilkan benar-benar sesuai kebutuhan dan kondisi yang ada di masyarakat Indonesia saat ini.
Pertama, murah. Saat ini dampak virus corona sangat dirasakan berbagai lapisan masyarakat sehingga kalau seseorang harus mendapat vaksinasi, alangkah harganya murah.
Tampaknya perlu dipikirkan biaya yang harus dikeluarkan untuk vaksinasi virus corona sangat terjangkau sesuai kondisi ekonomi masyarakat saat ini. Bahkan--jika mungkin--digratiskan atau ada subsidi.
Dalam kondisi dan situasi perekonomian masyarakat yang sangat terdampak wabah ini, Pemerintah Brazil berencana menggratiskan vaksin untuk masyarakat yang membutuhkan.
Pertimbangannya, kalau masyarakat sehat dan bebas dari cengkeraman virus ini maka ekonomi segera pulih. Pulihnya perekonomian warga adalah cermin perekonomian sebuah negara.
Kedua, cakupan (coverage). Vaksin ini diyakini sebagai upaya ampuh untuk mengendalikan virus corona.
Namun cakupan vaksinasinya perlu dipertimbangkan apakah hanya untuk bayi baru lahir, balita, remaja, orang tua atau lanjut usia? Begitu juga apakah hanya akan diberikan kepada orang yang pernah terinfeksi virus corona atau sedang mendapat perawatan karena virus ini?
Ataukah sebuah keharusan/kewajiban sehingga semua warga mendapat vaksinasi virus ini? Ataukah hanya untuk waktu-waktu tertentu saja seperti kewajiban meningitis untuk warga yang akan beribadah umrah dan berhaji?
Ketiga, aman. Aturan telah mengharuskan bahwa makanan, minuman dan--terlebih--obat bisa/boleh diberikan atau diedarkan jika aman dikonsumsi. Obat yang diedarkan harus terlebih dahulu lolos semua uji klinis sehingga diketahui dampak atau efek sampingnya.
Makanan, minuman dan obat dikatakan aman dikonsumsi sangat dipengaruhi prosesnya (termasuk peralatan) serta bahan yang digunakan.
Sampai saat ini, di Indonesia sudah banyak vaksin yang diberikan kepada masyarakat. Biayapun dari yang digratiskan, dikenakan harga murah dan terjangkau hingga cukup mahal.
Namun harus diakui masih ada sebagian warga yang tidak mau mendapat/menerima vaksinasi atau imunisasi dengan alasan tertentu. Alasannya dari soal biaya hingga masalah jaminan "keamanan".
Beberapa waktu lalu--sebelum ada wabah virus corona--masalah ini pernah mencuat. Alasannya lebih pada soal keraguan dan jaminan "keamanan".
Pihak-pihak terkait tentu perlu membahas hal tersebut agar nantinya tidak timbul perdebatan terkait harga, cakupan dan jaminan "keamanan".
Tampaknya tidak masalah bila soal seluk-beluk calon vaksin ini dibahas lebih luas dan mendalam agar ada pemahaman di publik.
Agar vaksin yang nanti dihasilkan benar-benar versi Indonesia yang secara uji klinis sesuai dengan kondisi dan kebutuhan masyarakat.
Menlu: produksi vaksin COVID-19 ditargetkan awal 2021
Pewarta: Sri Muryono
Editor: Ganet Dirgantara
Copyright © ANTARA 2020